|
COMPORTAMIENTO, DESCRIPCION Y TIEMPO DE DESARROLLO DE LOS ESTADOS
INMADUROSDE Eiphosoma vitticolle Cresson (HYMENOPTERA: ICHNEUMONIDAE),
PARASITO DE Spodoptera frugiperda (J. E. Smith)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
RESUMENPalabras claves: Eiphosoma vitticolle, comportamiento, descripción, tiem-po de desarrollo, estados inmaduros, huevo, larva, pupa. INTRODUCCIONEl énfasis creciente del control biológico en el manejo integrado de plagas demanda un gran conocimiento de la biología básica de los enemigos naturales y así como de la forma en que ellos interactúan con sus hospederos. Generalmente, el corion de los huevos es más o menos transparente y liso. Esto es cierto en la mayoría de los himenópteros endoparásitos, pero entre los ectoparásitos los huevos son a menudo tuberculados, reticulados, e incluso pueden ser espinosos. El color usual de los huevos en los insectos parásitos es blanco lechoso o amarillo pálido, pero algunos son amarillo intenso, anaranjado y ocasionalmente negros. Existen larvas primarias en himenópteros endoparásitos que a menudo poseen una combinación de varias características larvales. Algunas son mandibuladas y vesiculadas. Las formas de estas diferentes larvas son producto de la adaptación a medios especiales y las estructuras únicas obvias a menudo ofrecen una clave sobre cual es su función. Estas funciones están expresadas por características morfológicas en la larva que incluyen la locomoción, protección, ingestión y respiración (HAGEN, 1978). Los ichneumónidos presentan mucha diversidad en la estructura mandibular de las larvas. La mandíbula es ancha en la base, siendo el ápice muy puntiagudo, raras veces el ápice es bífido. En la mayoría de los ectoparásitos las mandíbulas presentan dientes sobre el filo y son aparentemente necesarios para mantenerse adherido al hospedero y horadar su piel, mientras que en la mayoría de los endoparásitos de este grupo no existen dientes en la mandíbula (BEIRNE, 1941; SHORT, 1959). La cápsula cefálica del último instar se encuentra siempre en el ápice del abdomen, junto a un saco membranoso que corresponde a la membrana peritrófica. En el estudio de varios himenópteros parásitos, principalmente entre Ichneumonidae y Braconidae, los investigadores han encontrado que las estructuras y otros detalles de la cápsula cefálica del último instar son muy útiles en la determinación de ciertas especies o para separar a muchos himenópteros en este estado (BEIRNE, 1941; SHORT, 1952, 1959; FINLAYSON, 1960; SHORT, 1970, 1976, 1977, 1978; FINLAYSON, 1967, 1975; citados por GILLESPIE y FINLAYSON, 1983; FINLAYSON y HAGEN, 1977; DIAZ, 1989 y GIRALDO-VANEGAS y GARCIA, 1992b). MORRIS (1937) indica que el número de instares entre los Hymenóptera Parasítica es variable, cinco parece ser lo más común y lo cual probablemente representa la condición más primitiva, ya que Symphyta presenta este número. El mismo autor sugiere que un instar se pierde en el desarrollo de los ichneumónidos y el estado de prepupa representa el quinto instar perdido. En Ichneumonoidea, la mayoría tienen cinco instares, aunque en algunos géneros se pueden presentar cuatro. Sin embargo, algunos Hyposoter spp parece que tienen sólo tres, mientras que en otras especies del mismo género ha sido claramente demostrado que tienen cinco (MUESEBECK y PARKER, 1933). En Braconidae se presentan variaciones similares dentro del género Bracon spp, pero en Cotesia spp todas las especies estudiadas han tenido solo tres instares (HAGEN, 1978). GIRALDO-VANEGAS y GARCIA (1992a) determinaron que E. vitticolle pasa por cuatro instares en su desarrollo larval y el quinto instar es reemplazado por un estado prepupal con dos fases, la eoninfal y la proninfal. El objetivo de este trabajo es descubrir los estados inmaduros y el tiempo de desarrollo de este insecto, criado en larvas de S. frugiperda. MATERIALES Y METODOSTres mil larvas de S. frugiperda, de seis días de edad, fueron expuestas a 20 hembras copuladas del parásito E. vitticolle, de siete días de edad (150 larvas del hospedero por hembra del parásito por jaula), por un período de seis horas, de 8 am a 2 pm. Al término del tiempo de exposición, fueron retirados los parásitos y se individualizaron las larvas de S. frugiperda en vasos plásticos de 25 ml, suministrándoles dieta artificial (GARCIA, 1981) para su alimentación. Individualizadas todas las larvas, éstas se colocaron en una cámara climática a 24.5 1.0oC, con humedad relativa de 76.0 10.0% y un fotoperíodo con luz artificial de 12 horas, de 6 am a 6 pm. Diariamente, desde el momento de la oviposición, se disecaban en Solución Ringer 60 larvas escogidas al azar; luego, con la ayuda de dos pinzas de punta fina, rasgando el integumento de la larva hospedera, se realizaban las observaciones con una lupa estereoscópica. Una vez localizados los huevos o larvas del parásito, se pasaban a un porta-objeto para su medición; en el caso de los huevos, el largo total y el ancho máximo, y en las larvas el largo total, largo del apéndice caudal y el ancho a nivel del primer segmento torácico. Para observar los estados de prepupa y pupa, diariamente se abrían longitudinalmente 20 capullos sacando la prepupa o pupa respectiva, realizando estas disecciones hasta que dejaran de emerger adultos del parásito, y de esta forma determinar la duración de los estados de prepupa y pupa, procediendo igualmente a medir el largo total y ancho a nivel del primer segmento torácico, anotando las características morfológicas respectivas. RESULTADOS Y DISCUSIONSe determinó que el promedio de duración del ciclo de vida de E. vitticolle, bajo condiciones de laboratorio (24.5 1.0oC de temperatura y una humedad relativa de 76.0 10.0%), desde la oviposición hasta la emergencia de los adultos, fue de 27.85 1.48 días. HuevoLas hembras de E. vitticolle depositan sus huevos directamente dentro del hemocelo del hospedero (Figura 1), donde ellos flotan libremente, hasta ubicarse en el extremo posterior del cuerpo, siendo estos transportados por la hemolinfa. Estas observaciones son consistentes con otras reseñadas para otros himenópteros endoparásitos que ovipositan en el hemocelo (FISHER, 1971). ARTHUR y MASON (1985), trabajando con el Ichneumonidae Banchus flavescens Cresson, encontraron que los huevos son ovipositados dentro del hemocelo de su hospedero Mamestra configurata L. (Lepidoptera: Noctuidae).
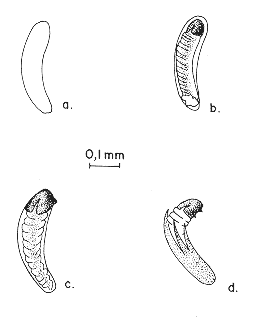
Los huevos recién ovipositados son del tipo himenopteriforme (CLAUSEN, 1940); alargados, lisos, en forma de bate corto y redondeado en ambos extremos; uno de los extremos es ligeramente más ancho y suavemente curvado en la parte media (Figura 2a), de un color beige traslúcido, siendo su longitud media, justamente recién ovipositado, de 0.366 0.02 mm y el ancho máximo de 0.102 0.04 mm (Cuadro 1). Al primer día de desarrollo, el embrión puede ser visible a través del corion (Figura 2b); mide 0.408 0.01 mm de largo y 0.119 0.02 mm de ancho (Cuadro 1); su color es marrón claro. Al segundo día de la oviposición ya se encontraron las primeras larvas en el momento de la eclosión, con la cabeza hacia la parte más ancha y las mandíbulas fuera del huevo, rompiendo el corion (Figura 2c); otras larvas fueron encontradas con la parte media anterior fuera del huevo y el corion roto longitudinalmente, pero aún adherido a la parte posterior de su cuerpo (Figura 2d).
Una vez que la larva rompe el corion con sus mandíbulas comienza a moverse dentro del huevo para permitir la imbibición del fluido que está a su alrededor; esta entrada de fluido externo probablemente ayude a la ruptura longitudinal del corion, para que de esta forma la larva pueda liberarse de él, facilitando su emergencia. La longitud promedio de los huevos para esta etapa de desarrollo fue de 0.420 0.01 mm y el ancho máximo de 0.123 ± 0.01 mm (Cuadro 1).
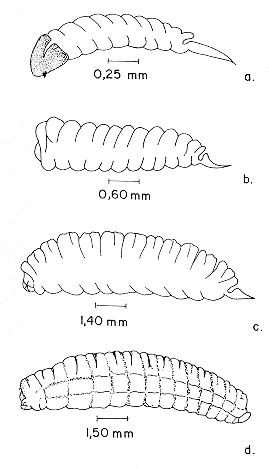
WILSON y RIDGWAY (1975), trabajando con el Ichneumonidae Campoletis sonorensis (Cameron), encontraron que la ruptura del corion fue hecha por las mandíbulas, simultaneamente con la presión ejercida por la hinchazón de la larva. A las 72 horas de desarrollo (tercer día de haber sido ovipuestos), los huevos miden 0.427 0.02 mm de largo y 0.130 0.01 mm de ancho (Cuadro 1); su color es marrón. Para el cuarto día de desarrollo (96 horas de incubación), el huevo mide 0.433 0.01 mm de largo y 0.136 0.02 mm de ancho (Cuadro 1), presentando un color marrón oscuro. La duración total del estado de huevo de E. vitticolle fue de 2.06 1.08 días. LarvaPrimer instar. La larva es de tipo caudada-mandibulada (CLAUSEN, 1940), lisa, hialina y brillante, sin pelos ni procesos. Su cuerpo está compuesto por 13 segmentos, tres torácicos y diez abdominales, completamente circulares, siendo ahusado hacia la parte posterior. Del último segmento abdominal se proyecta un largo y delgado apéndice caudal de forma cónica (Figura 3a), que representa el 29% de la longitud total de su cuerpo. Recién emergida, la larva tiene los segmentos torácicos del mismo ancho que la base de la cápsula cefálica. En este instar su cabeza es esférica, bien definida y esclerotizada, con dos invaginaciones laterales que le sirven para que la cabeza se amplíe con el crecimiento exagerado de este primer instar en su etapa final de desarrollo. Las mandíbulas en forma de hoz están localizadas ventralmente (Figura 4), presentando una mayor curvatura que en los instares subsiguientes, con una longitud promedio de 20.0 ± 0.80 micras (µ); el ancho de su base es de 12.30 2.90 micras (µ) (GIRALDO-VANEGAS y GARCIA, 1992a). FISHER (1971) hace la observación de que las mandíbulas en este primer instar, son usadas como garfios para adherirse a órganos o tejidos del hospedero, no siendo utilizadas para la alimentación como órganos masticadores. Después de la emergencia, la larva de E. vitticolle se desarrolla lentamente en los nueve primeros días, incrementando en tamaño solamente 1.32 mm/día. Inicialmente se alimenta de nutrimentos de la hemolinfa por absorción cuticular (HAGEN, 1978). CORBET (1968), trabajando con el Ichneumonidae Nemeritis canescens (Grav.), endoparásito de Ephestia kuehniella Zeller, encontró que la alimentación en el primer instar es realizada por la secreción de enzimas citolíticas de las glándulas salivales e intestino anterior, con la inmediata ingestión de la hemolinfa del hospedero por medio de una bomba faringeal. Observaciones similares sobre este modo de alimentación de himenópteros endoparásitos hacen VINSON y BARRAS (1970), trabajando con el Braconidae Cardiochiles nigriceps Viereck y WILSON y RIDGWAY (1975), con el Ichneumonidae Campoletis sonorensis (Cameron), ambos parásitos de larvas de Heliothis virescens (Fabricius). La ausencia de daños en órganos vitales del hospedero en esta primera etapa, explica la ausencia de efectos adversos visibles en el desarrollo de los hospederos parasitados. Las larvas se mueven dentro del hemocelo de su hospedero, ayudadas por su "cola" o apéndice caudal (CLAUSEN, 1940; HAGEN, 1978), hasta ubicarse a nivel de los tubos de Malpighi (WILSON y RIDGWAY, 1975).
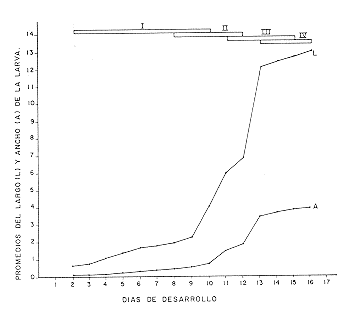
Este primer instar tiene una longitud promedio de 1.73 0.99 mm y el ancho a nivel del primer segmento torácico es de 0.32 0.18 mm (Cuadro 2). Este instar se encontró a partir del segundo día de la oviposición hasta el décimo día (Figura 5), con una duración promedio de 4.49 2.51 días (Cuadro 3).
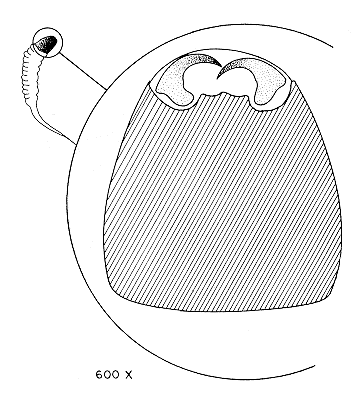
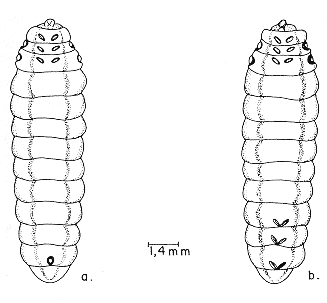
Segundo instar. Este se distingue fácilmente del primer instar por la pérdida de la cápsula cefálica, siendo en este instar poco esclerotizada, de forma semiesférica, retraída en los segmentos torácicos; el color del cuerpo es blanquecino, con 13 segmentos, conservando el apéndice caudal el cual representa el 5% de la longitud total del cuerpo (Figura 3b). A partir de este instar, las mandíbulas se localizan frontalmente, presentando una longitud promedio de 52.30 0.20 µ y 31.60 0.90 µ de ancho (GIRALDO-VANEGAS y GARCIA, 1992a). En las larvas del parásito se observa el tubo digestivo de color verde claro, debido posiblemente a que ha empezado a alimentarse de otras fuentes distintas a la hemolinfa. FISHER (1971) y WILSON y RIDGWAY (1975), consideran que el segundo instar de himenópteros endoparásitos inicia una alimentación combinada de hemolinfa y tejido adiposo. Un aumento considerable en la tasa de crecimiento de las larvas de E. vitticolle ocurre a partir del décimo día hasta el treceavo (Figura 5), incrementándose 6.30 mm por día; por lo que el desarrollo del hospedero comienza a ser obstaculizado. La longitud promedio de este instar fue de 3.89 0.43 mm y el ancho del primer segmento torácico fue de 1.96 ± 0.16 mm (Cuadro 2). Este segundo instar se consiguió desde el octavo día de la oviposición hasta el día doceavo (Figura 5), con una duración promedio de 2.84 1.40 días (Cuadro 3). Tercer instar. Este instar es similar al segundo, variando en la coloración del cuerpo que es amarillo claro, además, externamente ya no se observa el tubo digestivo. Todos los segmentos, torácicos y abdominales, presentan una apariencia un poco más plegados que el instar anterior. Su apéndice caudal sólo representa un poco menos del 1% de la longitud total del cuerpo (Figura 3). Las mandíbulas tienen una longitud promedio de 72.0 0.40 µ y 54.20 0.70 µ de ancho (GIRALDO-VANEGAS y GARCIA, 1992a). Para esta etapa de desarrollo, el cuerpo graso del hospedero se presenta granulado y lechoso. BARTELL y PASS (1978, 1980), trabajando con Bathyplectes curculionis (Thomson) y Bathyplectes anurus (Thomson), ichneumonidos, parásitos del picudo de la alfalfa, Hypera postica (Gyllenhal), encontraron que esto se debe a una respuesta del hospedero, ya que el parásito cambia la alimentación de hemolinfa a tejido adiposo. La longitud total del cuerpo fue de 11.03 0.80 mm, mientras que el ancho fue de 3.12 0.23 mm (Cuadro 2). Larvas de este instar se encontraron desde el día onceavo de la oviposición hasta el quinceavo día (Figrua 5), determinándose una duración promedio de 2.89 1.33 días (Cuadro 3). Cuarto instar. Las larvas son de color rosado y comprimidas dorso-ventralmente, siendo notorios unos lóbulos membranosos laterales en todos los segmentos del cuerpo. Se observa la zona pleural muy definida. Los espiráculos son visibles fácilmente, en número de nueve pares, un par en el protórax y los ocho restantes en los segmentos abdominales primero hasta el octavo, siendo este sistema respiratorio del tipo peripneústico (HAGEN, 1978). El apéndice caudal queda reducido a un pequeño lóbulo ventral, por encima del cual se localiza el ano (Figura 3) aún no funcional. En los segmentos torácicos, segundo y tercero, lateralmente se encuentran dos pares de depresiones redondeadas que corresponden a los rudimentos alares. Ventralmente, en una posición distomedial, en los segmentos torácicos se hallan tres pares de depresiones ovoides, que marcan la posición de los rudimentos de las patas (Figura 62a, 6b). Los sexos son fácilmente separables en este instar, ya que el macho posee en la parte ventral una depresión circular en la linea medial, cerca del margen posterior del segmento doceavo (Figura 6a); mientras que la hembra presenta tres pares de depresiones ovoides ventromediales en los segmentos décimo, onceavo y doceavo, cerca de los márgenes posteriores (Figura 6b). Las mandíbulas están fuertemente esclerotizadas y suavemente curvadas, midiendo 90.0 1.0µ de largo y 76.68 3.90 µ de ancho (GIRALDO-VANEGAS y GARCIA 1992a). Las dimensiones de este último instar fueron de 12.58 ± 0.38 mm de longitud y 3.74 0.20 de ancho (Cuadro 2). Este cuarto instar se halló desde el trecavo día de la oviposición hasta el día dieciseisavo (Figura 5), teniendo una duración promedio de 2.64 1.11 días (Cuadro 3). Faltando uno a dos días para que la larva parasítica abandone su hospedero, este se introduce en la dieta artificial, entra en estado de prepupa y prepara su celda pupal. La larva de E. vitticolle termina por consumir completamente todos los órganos del hospedero, quedando solamente fo-rrada por el integumento de este. La larva del parásito, justamente antes de salir del hospedero, se encuentra en una posición contraria, o sea, con la cabeza hacia la parte posterior del hospedero; ésta rompe con sus mandíbulas el integumento y sale por la parte ventral, entre las propatas de los segmentos VI y X; una vez fuera, comienza inmediatamente a tejer su propio capullo.
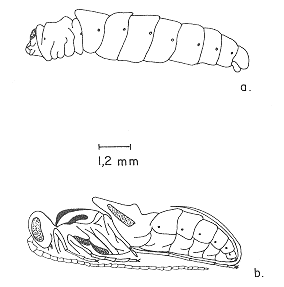
PupaUna vez la larva dentro del capullo, comienza a tener algunas modificaciones antes de llegar al estado de pupa. Estra transición prepupal tuvo una duración de 1.12 ± 0.33 días (Cuadro 4), presentando E. vitticolle dos fases: una primera fase, la eoninfal que es similar al cuarto instar con la diferencia que ha perdido los lóbulos membranosos laterales del cuerpo y la coloración rosada se torna más pálida; la segunda fase, la proninfal, poco móvil, de color amarillo pálido, es indicada por la aparición de ojos ima-ginales tenuamente visibles. La cabeza, el tórax y el abdomen, comienzan a diferenciarse por constricciones marcadas entre estas regiones (Figura 7a), siendo su longitud de 9.24 ± 0.43 mm y el ancho del primer segmento torácico de 3.16 ± 0.22 mm (Cuadro 5). La pupa es de tipo exarate (CLAUSEN, 1940; HAGEN, 1978). Las antenas se encuentran ventralmente dirigidas hacia el ápice del abdomen; los tarsos de las patas traseras llegan hasta el ápice del abdomen. El segundo segmento abdominal (peciolo) está doblado hacia arriba sobre el primer segmento abdominal (propodeo), luego, el tercer segmento está sobre el peciolo, continuando el resto del abdomen. El ovipositor en las hembras se encuentra curvado hacia arriba, descansando sobre el dorso del abdomen (Figura 7b). La pupa ya formada presenta ojos rojos prominentes; de color general blanco brillante, tornándose amarillo ocre a medida que avanza su desarrollo. La pupa mide en promedio 8.17 ± 0.33 mm de largo y 2.48 ± 0.15 mm de ancho (Cuadro 5). Completado el estado de pupa, a los 11.81 ± 0.88 días (Cuadro 4) el adulto rompe con sus mandíbulas el capullo por el extremo opuesto donde ha quedado adherido el integumento del hospedero, emergiendo el adulto para reposar, extender sus alas, endurecer la cutícula, dedicándose a la limpieza de su cuerpo.
SUMMARYKey words: Eiphosoma vitticolle, behavior, description, developmental time,inmature stages, egg, larva, pupa. BIBLIOGRAFIAARTHUR, A.P. and P.G. MASON. 1985. The life history and inmature stages of Banchus flavescens (Hymenoptera : Ichneumonidae) a parasitoid of the Bertha armyworm, Mamestra configurata (Lepidoptera : Noctuidae) in Westerm Canada. Can. Entom. 117:1249-1255. BARTELL, D.P. and B.C. PASS. 1978. Effects of Bathyplectes curculionis and Bathyplectes anurus (Hym. : Ichneumonidae) on the growth and development of Hypera postica (Coleoptera : Curculionidae). Enthomophaga 23(3): 281-291. BARTELL, D.P. and B.C. PASS. 1980. Morphology development, and behavoir of the inmature stages of the pasasite Bathyplectes anurus (Hym. : Ichneumonidae). Can. Entomol. 112:481-487. BEIRNE, B.P. 1941. A consideration of the cephalic structures and spiracles of the final instar larvae of the Ichneumonidae (Hym.). Trans. Soc. Brit. Ent. 7:123-190. CLAUSEN, C.P. 1940. Entomophagous insects. McGraw-Hill Book Co., Inc., New York and London. 688 p. CORBET, S.A. 1968. The influence of Ephestia kuehniella on the development of its parasite Nemetris canescens. J. Exp. Biol. 48:291-304. DIAZ B., F.A. 1989. Catálogo de los Ichneumonidae de Venezuela : Lista Inicial. Resúmenes XI Congreso Venezolano de Entomología. Maracaibo 5-8 de julio de 1989. FINLAYSON, T. 1960. Taxonomy of cocoons and puparia, and their contents, of Canadian Parasites of Neodiprion sertifer (Geoff.) (Hymenoptera : Diprionidae). Can. Ent. 92:20-47. FINLAYSON, T. and K.S. HAGEN. 1977. Final instar larvae of parasitic Hymenoptera. Simon Fraser University. Canada Pest Managament Paper Nº 10. 111 p. FISHER, R.C. 1971. Aspects of the physiology of endoparasitic Hymenoptera. Biol. Rev. 46:243-278. GARCIA R., J.L. 1981. Comparación del desarrollo de Spodoptera frugiperda (J.E. Smith) (Lepidoptera : Noctuidae), criado sobre una dieta artificial y sobre maíz. Bol. Entomol. Venez. 1(11):131-137. GILLESPIE, D.R. and T. FINLAYSON. 1983. Classification of final-instar of the Ichneumonidae (Hymenoptera : Ichneumonidae). Mem. Ent. Soc. Can. Nº 124. GIRALDO-VANEGAS, H. y J.L. GARCIA. 1992a. Determinación del número de instares de Eiphosoma vitticolle Cresson (Hymenoptera : Ichneumonidae). Bol. Entomol. Venez. N.S. 7(2):133-137. GIRALDO-VANEGAS, H. y J.L. GARCIA. 1992b. Morfología de la cabeza de larvas del cuarto instar de Eiphosoma vitticolle Cresson (Hymenoptera : Ichneumonidae). Rev. Fac. Agronomía 18(3-4):433-438. HAGEN, K.S. 1978. Estados de desarrollo de los parásitos. Cap. 7. In: Control biológico de las plagas de insectos y malas hierbas. P. De Bach (ed.). C.E.C.S.A. 6º Impresión. Mexico. pp. 205-282. MORRIS, K.R.S. 1937. The prepupal stage in Ichneumonidae, illustrated by the life-history of Exenterus abruptorius Thb. Bull. Ent. Res. 28:525-534. MUESEBECK, C.F.W. and P.L. PARKER. 1933. Hyposoter dispar Viereck, an introduced ichneumonid parasite of the gypsy moth. J. Agric. Res. 46:335-347. SHORT, J.R.T. 1952. The morphology of the head of larval Hymenoptera with special reference to the head of Ichneumonidea, including a classification of the final instar larvae of the Braconidae. The Transactions of the Royal Entomological Society of London. Vol. 103. Part. 2. pp. 27-84. SHORT, J.R.T. 1959. A description and classification of the final instar larvae of the Ichneumonidae. Proceeding of the United States National Museum. Vol. 110 Nº 3419. pp. 391-511. VINSON, S.B. and D.J. BARRAS. 1970. Effects of the parasitoid, Cardiochiles nigriceps, on the growth, development, and tissues of Heliothis virescens. J. Insect Physiol. 16:1329-1338. WILSON, D.D. and R.L. RIDGWAY. 1975. Morphology, development, and behavoir of the immature stages of the parasitoid, Campoletis sonorensis (Hymenoptera : Ichneumonidae). Ann. Ent. Soc. Am. 68(2):191-196 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||